Главните несакани ефекти на глукокортикоиди
Повеќегодишно искуство со глукокортикоидни лекови кај разни болести кај деца откри не само позитивни, туку и негативни аспекти на овој метод на терапија. Откриено е дека кај некои пациенти, несаканите реакции се привремени и малку изразени по природа и исчезнуваат без трага.
Кај другите деца, по укинувањето на глукокортикоидниот агенс, компликациите што се појавија, понекогаш многу тешки, траат многу години, а понекогаш и во текот на животот. Природата и сериозноста на несаканите реакции и компликации зависи од дневната доза и времетраењето на текот на третманот со глукокортикостероидни лекови, возраста на детето и индивидуалните карактеристики на реактивност на неговото тело.
Механизмите на несакани ефекти предизвикани од глукокортикостероиди се комплексни, бидејќи овие лекови ги напаѓаат сите аспекти на виталната активност на телото на детето. Сепак, несомнено може да се зборува за токсичните и алергиските ефекти на овие лекови, за нивната способност грубо да ја нарушат состојбата на имунитетот, да предизвикаат уништување на ткивата и да ги инхибираат процесите на регенерација во нив, значително да го вознемируваат метаболизмот. Несаканите реакции и компликации при третман на деца со глукокортикостероиди може да бидат како што следи.
1.Една од честите манифестации на хиперкортицизам на лекови што се вештачки создадени во телото на детето е Кушингоиден синдром: зголемување на телесната тежина со симптоми на чудна дебелина (заокружување на лицето, прекумерно таложење на маснотии на лицето, вратот, рамената, абдоменот) во комбинација со хипертрихоза, потење или сува кожа, нејзина пигментација, зголемена васкуларна шема на кожата, појава на акни и стрии.
Зголемената таложење на маснотии (машка дебелина од типот) е поврзана со катаболниот ефект на глукокортикостероидните лекови, зголемените процеси на глукокогеногенеза и пренамена на јаглехидрати во маснотии. Инхибиција на процеси за мобилизирање на масти стимулирани од хормон за раст е исто така важна.
2. Честа несакана реакција на администрацијата на глукокортикостероиди е таканаречениот стероиден гастритис, кој се манифестира со влошување на апетитот, металоиди, гадење, понекогаш повраќање, кисело белило, болка во епигастричниот регион.
Исто така е можно компликација во форма на ерозија и чиреви на желудникот и дуоденумот (тие исто така може да се појават во тенкото и тенкото црево). Чир на желудник и црево понекогаш се комплицирани со крварење и перфорација. Треба да се напомене дека чиревите на желудникот и цревата во почетните фази на нивното формирање можат да бидат асимптоматски, а знак на нивното постоење е позитивна реакција на окултната крв во измет.
Почесто, гастроинтестинални компликации се појавуваат по земањето глукокортикостероидни лекови внатре, иако нивниот развој не е исклучен со парентерална администрација на овие лекови. Појавата на улцеративен процес е најверојатно при препишување на преднизон и преднизон, особено во комбинација со други улцерогени агенси (имуносупресиви, ацетилсалицилна киселина, тетрациклини и др.).
Други фактори придонесуваат за развој на чиреви:
Преземање на глукокортикостероиди пред јадење,
Долготрајна администрација на високи дози на овие лекови без прекин во третманот,
· Неисполнување на диетата за време на терапијата со глукокортикостероиди (внес на зачинета и иритирачка храна, зачини, ладна или топла храна, итн.)
Глукокортикостероидите предизвикуваат формирање на чирови на желудникот и цревата поради следниве причини:
· Тие ја зголемуваат киселоста и секрецијата на желудечниот сок и истовремено го нарушуваат формирањето на слуз, кој ја штити мукозната мембрана на желудникот и цревата од штетни ефекти (инхибирана е синтезата на полисахариди кои ја сочинуваат мукозната мембрана на желудникот и цревата),
· Глукокортикостероидите ги ослабуваат процесите на заздравување на микро- и макро чиреви на желудникот и цревата, односно под нивно влијание е инхибирано размножувањето на клетките на жлездата и сврзното ткиво на theидовите на овие органи. Асимптоматскиот (безболен) тек на улцеративен процес се објаснува со фактот дека улцерацијата се јавува против позадината на антивоспалителното дејство на глукокортикостероидните лекови.
3. Во процесот на земање на глукокортикостероидни лекови, може да се забележи егзацербација на фокална инфекција (тонзилитис, синузитис, расипување на забите, холециститис и други), генерализација на инфективниот процес. Опишани се случаи на пневмонија и пулмонална супурација на автоинфективно потекло, егзацербација на хронични заболувања (хепатитис, холециститис, панкреатитис, туберкулоза и други).
Забележано е дека назначувањето на глукокортикостероиди предизвикува потежок тек на вирусни инфекции кај деца, драматично ја влошува ефикасноста на вакцинацијата. Несаканите ефекти наведени погоре се објаснети со можноста на глукокортикостероиди да ги потиснат системските и локалните одбранбени реакции.
4. Во третманот со глукокортикостероиди, можни се промени во менталната и емоционалната сфера: емоционална лабилност, логореја, психомоторна агитација, нарушување на спиењето. Овие промени кај децата се реверзибилни.
5. Честа несакана реакција со глукокортикостероидна терапија е зголемување на крвниот притисок. По испуштањето од болницата, поминува артериска хипертензија кај пациенти, иако кај некои деца е зголемено крвниот притисок за 15 - 20 mm RT. Уметност. опстојува од 1 до 3 години во отсуство на какви било поплаки (А. В. Долгополова, Н. Н. Кузмина, 1963).
Механизмот на артериска хипертензија при хиперкортицизам на лекови останува нејасен. Почесто, таквата реакција се евидентира кај предпебертална и пубертет.
6. Некои глукокортикостероиди (кортизон, хидрокортизон, преднизон, преднизон) имаат можност за задржување на натриум и вода во телото на пациентот, што придонесува за појава на едем и зголемување на телесната тежина. Ваквите глукокортикостероидни лекови како што се дексаметазон, триаминолон, метилпреднизолон не ги одложуваат натриумот и водата.
7.Со масивна и продолжена терапија со глукокортикостероиди кај адолесцентни девојчиња, често се забележани ендокрини нарушувања: доцнењето на појавата на првата менструација, нивната нерегуларност, кога веќе се утврдени. Неопходно е да се сметаат со ова и без строги индикации не ги пропишувајте овие лекови на девојчиња во периодот на пубертетот, откажете ги кога ќе се појават првите знаци на овие негативни појави.
8. Во литературата се дадени докази дека под влијание на долгорочно администрирање на глукокортикостероидни лекови може да се случи ретардација на растот на телото на детето. Овој феномен се објаснува со инхибиторниот ефект на глукокортикостероидите врз производството на хормон за раст од страна на хипофизата и формирање на соматомедин во црниот дроб, зголемување на катаболички процеси во ткивата, вклучително и коска.
9. Во детството, дијабетес мелитус може да се развие од влијанието на глукокортикостероидите од предјабетесот.
Механизмот на формирање на стероиден дијабетес е поврзан со карактеристики на дејство на глукокортикостероидни лекови врз метаболизмот на јаглени хидрати: тие ја инхибираат функцијата на изолациониот апарат на панкреасот, го стимулираат производството на плазма протеини кои се врзуваат за инсулин, го активираат процесот на формирање на глукоза од аминокиселини и во исто време ја ослабнуваат употребата на јаглени хидрати по ткива.
На крајот на краиштата, се развива хипергликемија и глукозорија, а кај деца со наследна ранливост на изолациониот апарат - дијабетес. Кај повеќето пациенти, по укинувањето на глукокортикостероидите, метаболизмот на јаглени хидрати се нормализира. Дексаметазон е во состојба да предизвика особено изразени нарушувања во метаболизмот на јаглени хидрати, помалку од триаминолон, метилпреднизолон, преднизолон, преднизон. Минималната дијабетогеност е карактеристична за кортизон и хидрокортизон.
10. Честа несакана реакција на телото на детето на администрација на глукокортикостероиди е зголемена екскреција на калиум во урината и развој на хипокалемичен синдром.
Знаци на второто: чувство на слабост, малаксаност, губење на мускулниот тонус и јачина (понекогаш пареза на екстремитетите), слабеење на функцијата на миокардот, срцева аритмија, гадење, повраќање, запек.
Можноста за развој на хипокалемичен синдром се зголемува со администрација на глукокортикостероиди во комбинација со срцеви гликозиди и диуретици, притоа да се игнорира диета на калиум и недоволна компензација за фармакогени загуби на калиум заради дополнителна администрација на лекови за хемотерапија што содржат калиум.
11. Направени се многу клинички наб observудувања што укажуваат на негативните ефекти на глукокортикостероидните лекови врз скелетниот систем на растечкото тело на детето. Стероидна остеопатија е изразена при појава на остеопороза на претежно долги тубуларни коски, ребра и вертебрални тела. Честопати, развојот на епифизална 'рскавица е нарушен, понекогаш се појавуваат знаци на асептична некроза на коските.
Многу сериозна компликација е бревиспондилијата: формирање на рибни пршлени (поради уништување на вертебралните тела и интервертебралните дискови), проследено со можно кршење на нервните корени, фрактура на 'рбетот и компресија на' рбетниот мозок.
Стероидна остеопатија е резултат на груби нарушувања во синтезата на протеинските структури на коскеното ткиво (намалување на количината на колаген, мукополисахариди, хексасамин), зголемени процеси на реапсорпција на калциум од коскеното ткиво и прекумерно излачување на него и фосфор во урината. Репаративните процеси во коскеното ткиво кај пациенти со стероидна остеопатија се карактеризираат со летаргија и времетраење.
12. Кај некои пациенти, миопатијата се развива под влијание на глукокортикостероидни лекови.
Симптоми на неа: мускулна слабост (главно во проксималните долни екстремитети и мускулите на трупот), хипотензија, намалени рефлекси на тетива. На преглед, може да забележите знаци на хипертрофија на мускулите, особено на долните екстремитети (се зголемува содржината на гликоген во мускулите). Докажано е нарушување на структурата на невромускулните синапси. Триамцинолон што содржи флуор често предизвикува миопатија. Стероидна миопатија по повлекувањето на лекот постепено исчезнува, а функцијата и структурата на мускулите се обновуваат со празнина.
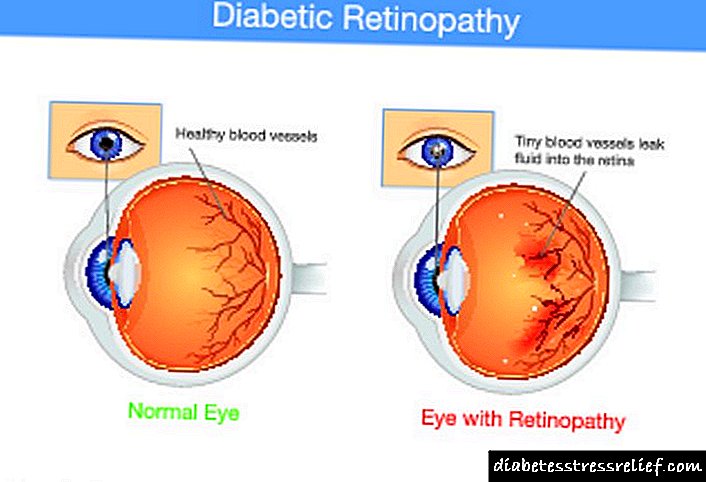
13. Употребата на глукокортикостероиди (особено во случаи на долгорочно администрирање масивни дози на лекови) е полн со опасност од компликации од органот на видот во форма на затнување на леќи и глауком. Промените во леќите може да станат неповратни поради кампулацијата на воден хумор, набивањето на задниот дел од неа. Глаукомот во детството е редок.
14. Иако глукокортикостероидните лекови се моќен терапевтски фактор кај алергиите, во некои случаи тие самите произведуваат алергиски реакции, до анафилактичен шок. Ваквите реакции често се случуваат со повторени курсеви на глукокортикостероидна терапија и се манифестираат во форма на уртикарија, едем на Квинке, еритема мултиформ, чешање на кожата и други знаци.
15. Долготрајната употреба на глукокортикостероидни лекови и како резултат на состојба на фармакогени хиперкортицизам е полн со опасност од инхибиција на функцијата на кортикалниот слој на надбубрежните жлезди и компензаторно реструктуирање на хипоталамо-гинефизијално-надбубрежниот систем.
Наспроти ова, со ненадејно повлекување на лекот, синдромот на повлекување може да се развие во форма на напад на силна слабост, слабост, главоболка, намалени ментални и физички перформанси и умерено зголемување на телесната температура.
Синдром на повлекување е особено опасен во случаи кога администрацијата на големи дози на глукокортикостероиди е запрена без претходна подготовка на телото на пациентот, имено, без постепено намалување на дневната доза на лекот, воведување на хемотерапевтски агенси кои ја стимулираат функцијата на надбубрежниот кортекс.
Така, групата на глукокортикостероидни лекови се карактеризира не само со неговите моќни терапевтски ефекти врз телото на пациентот, туку и со многу негативни феномени, чија сериозност и суштина зависи од самата дрога, од методот на неговата употреба, возраста и полот на детето и други фактори, за жал сè уште не е проучено.
Фармаколошката терапија за ХА може да биде интензивна (краткорочна), ограничена (неколку дена или месеци) и долгорочна (третман за неколку месеци, години, па дури и доживотно).
Не го најдовте она што го баравте? Користете го пребарувањето:
Несакани ефекти на системски глукокортикоиди
Содржина
Несакани ефекти
■ Инхибиција на функција и атрофија на надбубрежниот кортекс, стероидна зависност, „синдром на повлекување“ (егзацербација на основната болест, надбубрежна инсуфициенција). Долготрајната терапија со системски глукокортикоиди, особено спроведена без да се земат предвид физиолошки циркадијански ритами на нивната секреција, доведува до инхибиција и атрофија на надбубрежниот кортекс. За целосно инхибирање на надбубрежниот кортекс кај возрасен пациент, дневната доза на егзогени глукокортикоид треба да биде 10-20 mg во однос на преднизон. Намалувањето на функцијата на надбубрежниот кортекс започнува на 4 - 7-ти ден на дневна употреба на средни дози на глукокортикоиди кога се препишуваат наутро и од 2-ри ден кога се пропишани во вечерните часови. Овој несакан ефект е најкарактеристичен за долго дејство на оралните глукокортикоиди и препарати за складирање. За да се врати нормалната секреторен функција на надбубрежниот кортекс, потребни се најмалку 6-9 месеци, а нејзината соодветна реакција на стресот е до 1-2 години.
Inning Разредување на кожата, стрии, ќелавост.
■ Остеопороза, фрактури и асептична некроза на коските, ретардација на растот. Остеопорозата се развива кај 30-50% од пациентите и е најсериозна компликација на терапија со глукокортикоид. Тоа се должи на нивниот негативен ефект врз формирањето на коскеното ткиво и активирањето на неговата ресорпција. Често се развива кај жени во постменопаузалниот период. Како по правило, остеопорозата влијае на централните делови на скелетот ('рбетниот столб, карличните коски, ребрата) и постепено се шири на периферните коски (раце, стапала и сл.) .Нејзините клинички манифестации се болка во зглобовите на' рбетот и колкот, намален раст и фрактури на 'рбетот (долниот торакален и лумбалниот оддели), ребра, феморален врат, кои произлегуваат од помали повреди или спонтано. За лекување на оваа компликација, се користат препарати на калциум, витамин Д3, калцитонин и бифосфонати. Времетраењето на таквата терапија треба да биде неколку години.
• Миопатија, трошење на мускули, миокардна дистрофија. Стероидните миопатии се манифестираат со слабост и атрофија на скелетните мускули, вклучувајќи респираторни мускули (меѓуребрените мускули, дијафрагма), што придонесува за развој на респираторна слабост. Најчесто, оваа компликација предизвикува триамцинолон. Механизмот на развој на миопатија е поврзан со негативниот ефект на глукокортикоидите врз метаболизмот на протеините и минералите. За нивно лекување се користат анаболни стероиди и препарати од калиум.
■ Хипокалемија, задржување на натриум и вода, едем се манифестации на минералокортикоидните ефекти на глукокортикоидите.
■ Зголемување на крвниот притисок може да се забележи кај пациенти кои земаат глукокортикоиди подолго време. Се должи на зголемена чувствителност на васкуларниот wallид на катехоламини, задржување на натриум и вода.
■ Оштетување на васкуларниот wallид со развој на "стероиден васкулитис" честопати е предизвикано од флуорирани лекови (дексаметазон и триаминолон). Се карактеризира со зголемена васкуларна пропустливост. Се манифестира со хеморагии во кожата на подлактиците, мукозните мембрани на усната шуплина, конјунктивата на очите, епител на гастроинтестиналниот тракт. За третман, се користат витамини Ц и П, како и анти-брадикинин васкуларни агенси.
■ Зголемувањето на коагулабилноста на крвта може да доведе до формирање на згрутчување на крвта во длабоки вени и тромбоемболизам.
■ Забавување на регенерацијата на ткивата како резултат на анти-анаболни и катаболни ефекти врз метаболизмот на протеините - намалување на синтезата на протеини од аминокиселини, зајакнување на распаѓање на протеините.
■ Стероидни чиреви на желудникот и цревата, гастроинтестинално крварење. Стероидните чиреви често се асимптоматски или асимптоматски, манифестирајќи крварење и перфорација. Затоа, пациентите кои примаат орално глукокортикоиди подолго време треба да се испитуваат периодично (фиброезофагоастростродуоденоскопија, фекален окултен тест на крвта). Механизмот на улцерогено дејство на глукокортикоиди е поврзан со нивниот катаболен ефект и сузбивање на синтезата на простагландин и се состои во зголемување на секрецијата на хлороводородна киселина, намалување на формирање на слуз и инхибиција на регенерацијата на епителот. Оваа компликација почесто е предизвикана од преднизон.
■ Панкреатитис, масен црн дроб, дебелина, хиперлипидемија, хиперхолестеролемија, емболија на маснотиите се резултат на анаболниот ефект на глукокортикоидите врз метаболизмот на мастите - зголемена синтеза на триглицериди, масни киселини и холестерол, прераспределување на маснотиите.
■ Зголемена ексцитабилност на ЦНС, несоница, еуфорија, депресија, психоза, симптоми на менингизам, напади на пациенти со епилепсија.
Постериран субкапсуларен катаракта, глауком, егзофталмос.
■ стероиден дијабетес, хипергликемија. Глукокортикоидите ја зголемуваат апсорпцијата на јаглехидратите од гастроинтестиналниот тракт, ја зајакнуваат глуконогенезата, ја намалуваат активноста на инсулин и хексокиназа и ја намалуваат чувствителноста на ткивата кон инсулин и нивната употреба на гликоза. За третман на стероиден дијабетес, се користи диета ограничена со јаглени хидрати, орални хипогликемични лекови и инсулин.
■ Прекршување на менструалниот циклус, сексуалните функции, одложен сексуален развој, хирзутизам, нарушен развој на фетусот се поврзани со намалување на производството на полови хормони.
■ Задушување на имунитетот, егзацербација на хронични инфективни и воспалителни процеси, вклучително и туберкулоза, секундарна инфекција, генерализација на локална инфекција. Како по правило, заразни компликации се асимптоматски како резултат на антиинфламаторно дејство на глукокортикоиди. Карактеристичен е развојот на кандидијаза на усната шуплина и фаринксот.
Syndrome Кушингов синдром (мобилизација на маснотии од поткожното масно ткиво на екстремитетите, прекумерно таложење на маснотии во лицето, вратот, зглобот на рамото и абдоменот, хипертрихоза, стрии, акни, нарушена толеранција на гликоза, итн.)
■ Хематолошки промени.
■ Манифестиран со неутрофилна леукоцитоза без промена на формулата на леукоцити лево. Се верува дека тие се должат на стимулирачкиот ефект на стероидите врз гранулопоезата.
Спречување на компликации
■ Употреба на режим на наизменично (наизменично) лекување.
■ Употреба на системски глукокортикоиди во минималната потребна доза. За ова, кај бронхијална астма, нивната администрација треба да се комбинира со употреба на инхалирани глукокортикоиди во комбинација со долготрајни β2-адренергични агонисти, теофилин или антилеукотриен.
■ администрација на глукокортикоиди во согласност со физиолошки дневен ритам на секреција на кортизол.
■ Употреба на диета богата со протеини и калциум, со ограничување на лесно сварливи јаглени хидрати, сол (до 5 g на ден) и течност (до 1,5 литри на ден).
■ Земање таблети глукокортикоиди после јадење за да се намали нивниот улцероген ефект.
■ Елиминација на пушење и злоупотреба на алкохол.
■ Умерено нетрауматско вежбање.
Концептот на глукокортикоиди, нивната употреба како лекови, класификација според структурата и дејството. Начини на регулирање на синтезата и секрецијата на хормоните на надбубрежниот кортекс Механизмот на дејство на глукокортикоидите, главните несакани ефекти од нивната употреба.
| Наслов | Медицина |
| Погледни | апстрактна |
| Јазик | Руски |
| Додаден датум | 22.05.2015 |
| Големина на датотеката | 485.1 К |

Доставувањето на вашата добра работа до базата на знаење е лесно. Користете ја формата подолу
Студентите, дипломираните студенти, младите научници кои ја користат базата на знаење во своите студии и работа ќе ви бидат многу благодарни.
Објавено на http://www.allbest.ru/
Министерство за здравство на Украина
Zaporizhzhya Државниот медицински универзитет
Одделение за фармакологија и медицински рецепт
Предмет: „Фармакологија“
На тема: „Несакани ефекти на глукокортикоиди“
Завршено: 3-годишно студент
Саико Роман Едуардович
1. Класификација на глукокортикоиди
2. Механизмот на дејство на глукокортикоиди
3. Употреба на глукокортикоиди
4. Главните несакани ефекти на глукокортикоиди
5. Превенција на несакани ефекти на глукокортикоиди
Список на референци
1.Класификација на глукокортикоидво
Глукокортикоидите се стероидни хормони кои се синтетизираат од кората на надбубрежните жлезди. Природните глукокортикоиди и нивните синтетички аналози се користат во медицината за надбубрежна инсуфициенција. Покрај тоа, некои болести користат антиинфламаторни, имуносупресивни, антиалергични, анти-шок и други својства на овие лекови.
Почетокот на употребата на глукокортикоиди како лекови (ПМ) датира од 40-тите години. XX век. Назад кон крајот на 30-тите години. од минатиот век, се покажа дека хормоналните соединенија од стероидна природа се формираат во кората на надбубрежните жлезди. Во 1937 година, минералокортикоидниот деоксикортикостерон беше изолиран од надбубрежниот кортекс, во 40-тите години. - глукокортикоиди кортизон и хидрокортизон. Широк спектар на фармаколошки ефекти на хидрокортизон и кортизон ја одредија можноста за нивна употреба како лекови. Наскоро, нивната синтеза беше извршена.
Главниот и најактивниот глукокортикоид формиран во човечкото тело е хидрокортизон (кортизол), други помалку активни се претставени со кортизон, кортикостерон, 11-деоксикортизол, 11-дехидрокортикостерон.
Производството на хормони од надбубрежните жлезди е под контрола на централниот нервен систем и е тесно поврзано со функцијата на хипофизата (види Сл. 2). Адренокортикотропен хипофизен хормон (ACTH, кортикотропин) е физиолошки стимулатор на кората на надбубрежните жлезди. Кортикотропинот го подобрува формирањето и секрецијата на глукокортикоиди. Вторите, пак, влијаат на хипофизата, спречувајќи го производството на кортикотропин и со тоа ја намалуваат понатамошната стимулација на надбубрежните жлезди (по принцип на негативни повратни информации). Продолжената администрација на глукокортикоиди (кортизон и неговите аналози) во организмот може да доведе до инхибиција и атрофија на надбубрежниот кортекс, како и до инхибиција на формирање не само на ACTH, туку и на гонадотропни и на тироидната жлезда-стимулирачки хормони.
Сл.Класификација на глукокортикоиди и методи за нивна употреба
Сл.Начини на регулирање на синтезата и секрецијата на хормоните на надбубрежниот кортекс
Од 50-тите години на минатиот век, глукокортикоидите заземаа значајно место во разни области на медицината и, пред сè, во терапевтската пракса. Синтезата на форми на глукокортикоиди за интравенска и интрамускулна администрација значително ги прошири можностите на глукокортикоидна терапија. Во текот на изминатите 15-20 години, нашите идеи за механизмите на дејствување на глукокортикоиди значително се проширија, а исто така има и сериозни промени во тактиката на користење глукокортикоиди, вклучувајќи дози, патишта на употреба, времетраење на употреба и комбинации со други лекови.
Употребата на глукокортикоиди во клиничката пракса датира од 1949 година, кога за прв пат е забележано одличниот краткорочен ефект на кортизон кај пациенти со ревматоиден артритис. Во 1950 година, истата истражувачка група известуваше за добрите резултати од третманот на ревматоиден артритис, ревматизам и други ревматски заболувања со кортизон и адренокортикотропен хормон (ACTH). Наскоро, серија извештаи покажаа брилијантен ефект на глукокортикоидна терапија за системски лупус еритематозус (СЛЕ), дерматомиозитис и системски васкулитис.
Денес, глукокортикоидите и покрај големиот ризик од несакани ефекти (вклучително и сериозни), остануваат камен темелник во патогенетскиот третман на многу ревматски заболувања. Покрај тоа, тие се користат во многу хематолошки заболувања, примарен и секундарен гломерулонефритис, како и во голем број на гастроинтестинални и респираторни заболувања, алергиски состојби, шокови од различно потекло и многу повеќе. Синтезата на глукокортикоиди за интравенска, интрамускулна и интраартикуларна употреба го прошири обемот и тактиката на нивната употреба.
Кортикостероиди на надбубрежните жлезди се поделени во две главни категории - глукокортикоиди и минералокортикоиди. Првите имаат ефект врз скоро сите органи и системи на телото, со тоа што влијаат на средните метаболички процеси, имуните функции и воспалителни реакции. Главната функција на минералокортикоидите е регулирање на метаболизмот со вода сол.
Распространетата употреба на глукокортикоиди е мотивирана од нивните моќни антиинфламаторни, имуносупресивни и антиалергиски ефекти.
На 1-ви Европски симпозиум за глукокортикоидна терапија, се препорачува употреба на термините глукокортикоиди или глукокортикостероиди. Други поими - „стероиди“, „кортикостероиди“, „кортикоиди“ се премногу широки или недоволно точни, и затоа не се препорачува нивно користење.
Во клиничката пракса денес се користат исклучиво синтетички глукокортикоиди, кои имаат значителна антиинфламаторна, имуносупресивна и антиалергиска активност со слаби или дури и нула минералокортикоидни ефекти, и затоа тие се едни од најчесто користените лекови во разни области на медицината.
Класификација на глукокортикоиди според хемиска структура
Природни (ендогени) глукокортикоиди:
* кортизол * хидрокортизон * хидрокортизон ацетат
Гликокортикоиди кои содржат синтетичко масло:
* преднизолон * преднизон * метилпреднизолон
Гинококортикоиди кои содржат синтетички флуор:
* дексаметазон * триамцинолон * бетаметазон
Класификација на глукокортикоиди според времетраењето на дејството
Лекови со кратко дејство (8-12 часа):
Лекови со просечно времетраење на дејството (12-36 часа):
* преднизолон * метилпреднизолон * триамцинолон
Долгорочни лекови (36-72 часа):
* параметарзон * бетаметазон * дексаметазон
Гликокортикоидите на депото се карактеризираат со подолга изложеност (елиминација во рок од неколку недели).
2.Крзноглукокортикоиден анизам
Оската на хипоталамо-хипофизата-надбубрежната форма формира комплексен систем кој го регулира ослободувањето на глукокортикоидите во физиолошки состојби и во различни патолошки состојби. Производството на кортизол од надбубрежниот кортекс е регулирано со ACTH, секретирано од предната хипофиза. Ослободувањето на ACTH, пак, е регулирано со коортикотропин ослободувачки хормон, чија секреција се контролира со невролошки, ендокрини и цитокински системи на ниво на перивентрикуларните јадра на хипоталамусот. Хормонот ослободен од кортикотропин се транспортира во мали делови до локалната портална циркулација на хипофизата, а потоа и во неговиот преден лобус, каде што хормонот ослободен од кортикотропин го стимулира лачењето на ACTH. глукокортикоидна страна на лекот
Дневната базална секреција на кортизол кај луѓето е околу 20 мг. Покрај тоа, неговата секреција се карактеризира со флуктуации во текот на денот со највисоко ниво во раните утрински часови и ниски вредности во вечерните часови. Најмногу секретираниот кортизол (околу 90%) циркулира со глобулини кои се врзуваат за кортикоид. Бесплатниот кортизол е биолошки активна форма на хормонот.
Хиперреактивноста на хипоталамо-хипофизата-надбубрежната оска во отсуство на воспаление (на пример, со синдром Кушингов) предизвикува имуносупресија и ја зголемува чувствителноста на инфекција. Активирање на хипоталамо-хипофизата-надбубрежната оска, предизвикувајќи зголемување на нивото на кортизол и да доведе до имуносупресија, може да биде предизвикано од разни стресни фактори, вклучувајќи болка, емоционална траума, студ, одличен физички напор, инфекции, хируршки интервенции, ограничување на ограничување на калории на храна и многу повеќе. Ендогени глукокортикоиди, заедно со хомеостатска улога, исто така, ги модифицираат антиинфламаторните реакции. Прикажани се докази дека нарушениот одговор на ендогени глукокортикоиди игра важна улога во патогенезата на голем број системски заболувања на сврзното ткиво или во упорноста на воспалителниот процес. Кај ревматските заболувања како што се ревматоиден артритис, СЛЕ, дерматомиозитис и други, значителни промени се случуваат во оската на хипоталамо-хипофизата-надбубрежната жлезда, што се карактеризира со несоодветно лачење на ACTH во однос на циркулираните цитокини, несоодветно ниско базално и стимулирано лачење на кортизол како одговор на воспаление, како и значително намалување андроген.
Употребата на синтетички глукокортикоиди доведува до инхибиција на синтезата и ослободување на двата хормони што ослободуваат кортикотропин и ACTH, и следствено на тоа, намалување на производството на кортизол. Долготрајната терапија со глукокортикоиди резултира во надбубрежна атрофија и сузбивање на хипоталамо-хипофизата-надбубрежната оска, предизвикувајќи намалување на можноста за производство на дополнителни ендогени глукокортикоиди како одговор на ACTH и стресни фактори.
Во моментов, вообичаено е да се прави разлика помеѓу два механизма на дејство на глукокортикоиди - геномски и не-геномски.
Геномскиот механизам преку врзување на специфични цитоплазматски рецептори се забележува во која било доза и се појавува не порано од 30 минути по формирањето на комплексот на хормони-рецептори.
Основниот механизам на геномското дејство на глукокортикоидите е регулирање на транскрипција на гените кои ја контролираат синтезата на протеините и ДНК. Ефектот на глукокортикоиди врз гликокортикоидните рецептори (кои се членови на мембранозен стероид рецептор), доведува до развој на комплекс на настани кои вклучуваат специфични РНК-месинџер, нуклеарна РНК и други супстанции за промотор. Резултатот од оваа каскада е стимулација или инхибиција на транскрипција на гени. Глукокортикоидите влијаат на голем број гени, вклучително и гени кои го контролираат формирањето на цитокини како што се IL-la, IL-4, IL-6, IL-9 и гама интерферон. Во овој случај, глукокортикоидите можат да ја подобрат транскрипцијата на гените и да ја потиснат.
Глукокортикоидите ја контролираат синтезата на клеточните протеини. Проникнувајќи лесно и брзо преку клеточните мембрани, тие формираат комплекси со стероидни рецептори во цитоплазмата кои мигрираат во клеточното јадро, при што се извршува транскрипција на генетскиот апарат.
специфичен гласник РНК за синтеза на регулаторни пептиди и протеини, првенствено поврзани со систем на ензими, кои, пак, ја контролираат клеточната функција.Овие ензими можат да вршат и стимулативни и инхибитивни функции. На пример, тие можат да го стимулираат производството на инхибиторни протеини во некои клетки, што целосно ја запира транскрипцијата на гените во лимфоидните клетки, а со тоа модулираат имунолошки и воспалителни реакции.
Глукокортикоидите влијаат врз клеточните и хуморалните имунолошки функции. Развојот на лимфоцитопенија под нивно влијание се должи на инхибиција на производство и ослободување на лимфоидни клетки од коскената срцевина, инхибиција на нивната миграција и прераспределување на лимфоцитите во други лимфоидни делови. Глукокортикоидите влијаат врз кооперативната интеракција на Т и Б клетките во имунолошкиот одговор. Тие различно делуваат на различни подпопулации на Т-лимфоцити, предизвикувајќи намалување на нивото на Т-клетките што носат рецептори за фрагментот IgM Fc и без промена на нивото на Т-лимфоцити кои носат рецептори за фрагментот IgG Fc. Под влијание на глукокортикоиди, пролиферативните способности на Т-клетките се потиснуваат и ин виво и ин витро. Ефектот на глукокортикоидите врз одговорите на Б-клетките се манифестира во помала мерка отколку на Т-клетките. Значи, кај пациенти кои примаат средни дози на глукокортикоиди, се забележуваат нормални реакции на антитела на имунизација. Во исто време, краткотрајната администрација на големи дози на глукокортикоиди предизвикува намалување на нивото на IgG и IgA во серумот и не влијае на нивото на IgM. Ефектот на глукокортикоиди врз функцијата на Б-клетките може да биде посредуван заради нивниот ефект врз макрофаги.
За разлика од геномските, негеномски ефекти на глукокортикоидите се резултат на директни физичкохемиски интеракции со биолошки мембрани и / или стероиди-селективни мембрани на рецептори. Не-геномски ефекти на глукокортикоиди се развиваат под влијание на повисоки дози и се појавуваат по неколку секунди или минути.
Не-геномското антиинфламаторно дејство на глукокортикоидите е поврзано со стабилизирање на лизозомалните мембрани, намалување на пропустливоста на клеточните мембрани, намалување на капиларна пропустливост и локален проток на крв во области на воспаление, намалување на оток на ендотелијални клетки, намалување на способноста на имуните комплекси да навлезат во подрумската мембрана, да го инхибираат и да го поттикнат синтезата на раст садови во фокусот на воспаление и намалување на нивната пропустливост (делумно се должи на
инхибиција на синтезата на простагландин), намалување на бројот на моноцити и мононуклеарни клетки во фокусот на воспалението, како и ефект врз полиморфоннуклеарните леукоцити. Очигледно, водечката улога во антиинфламаторниот ефект на глукокортикоиди припаѓа на инхибиција на миграција и акумулација на леукоцити во фокуси на воспаление. Под влијание на глукокортикоиди, бактерицидно дејство, врзување на Fc рецептор и други функции на моноцити и макрофаги се нарушени, а нивото на еозинофили, моноцити и лимфоцити во циркулацијата се намалува. Покрај тоа, клеточните реакции на кинини, хистамин, простагландини и хемотактички фактори се менуваат, а ослободувањето на простагландини од стимулираните клетки се намалува. Добро проучен негеномски механизам вклучува активирање на ендотелна синтазаза на азотен оксид.
Дозата на глукокортикоиди ја одредува нивната ефикасност, како и зачестеноста и сериозноста на несаканите ефекти. Геномските ефекти на глукокортикоидите се развиваат со минимални дози и се зголемуваат бидејќи се постигнуваат приближно 100 мг еквивалент преднизолон на ден, и остануваат стабилни во иднина. Ако при употреба на глукокортикоиди во доза до 30 мг преднизолонски еквивалент, терапевтскиот резултат е скоро целосно утврден со геномски механизми, тогаш во доза од повеќе од 30 мг преднизолонски еквивалентни не-геномски ефекти стануваат значајни, чија улога брзо се зголемува со зголемување на дозата.
Глукокортикоидите добро се реапсорбираат за сите варијанти на нивната употреба, т.е. за орални, интрамускулни, интравенски или интраартикуларни. По орална администрација, се апсорбираат околу 50-90% од глукокортикоиди. Врзаноста на глукокортикоидите со протеините во крвта е приближно 40-90%. Метаболизмот на глукокортикоидите се изведува главно во црниот дроб, а излачувањето - главно од бубрезите во форма на метаболити. Врвната концентрација на глукокортикоиди во крвта по орална администрација се јавува по 4-6 часа. Со интравенска администрација на глукокортикоиди, врвот на нивната концентрација се постигнува многу побрзо. Значи, со воведување на 1,0 Sol Solededrol® (метилпреднизолон натриум сукцинат), после 15 минути се забележува врв во неговата концентрација во плазмата. Со интрамускулна администрација на глукокортикоиди, врвот на нивната концентрација во плазмата се јавува значително
подоцна На пример, со интрамускулна инјекција на Депо-медрол® (метилпреднизолон ацетат), неговата максимална концентрација во крвта се постигнува по околу 7 часа.
3. Употреба на глукокортикоиди
Опишаните повеќеслојни механизми на дејство на глукокортикоиди и разни точки на нивната примена служеа како основа за нивна широко распространета употреба кај многу заболувања на внатрешните органи, како и голем број патолошки состојби. Заедно со ревматските заболувања и системскиот васкулитис, каде што глукокортикоидите често се основни лекови, глукокортикоидна терапија се користи и во ендокринологија, гастроентерологија, реанимација, кардиологија, пулмологија, нефрологија, трауматологија и друго.
Подолу ви претставуваме болести и патолошки состојби во кои се користат глукокортикоиди:
1.Ревматоиден артритис - во отсуство на сериозни вонпартикуларни манифестации на болеста (системски васкулитис, серозитис, миокардитис, фиброзирачки алвеолитис, бронхиолитис облитеранс), ниски дози на глукокортикоиди се користат против позадината на терапијата за менување на болести. Со развојот на горенаведените вонпартикуларни манифестации на ревматоиден артритис, се користат средни и, доколку е потребно, високи дози на глукокортикоиди.
2. Анкилозен спондилитис - во активна фаза се користат средни или високи дози на глукокортикоиди.
3. Системски лупус еритематозус - во активната фаза на болеста, како и кога виталните органи и системи се вклучени во патолошкиот процес (тежок перикардитис и / или плеврит со масивна акумулација на ексудат, и / или миокардитис, и / или оштетување на централниот нервен систем и / или пулмонален пневмонитис , и / или пулмонални крварења, и / или хемолитична анемија, и / или тромбоцитопенична пурпура, и / или активен глупулулонефритис III, IV, V, лупус) покажува употреба на средни или високи дози на глукокортикоиди и доколку е потребно - многу висока Ела.
4. Акутна ревматска треска или егзацербација на ревматизам - средни или високи дози на глукокортикоиди (особено со развој на ревматски кардитис).
5. Ревматска полимиалгија - глукокортикоиди се лекови по избор. Во акутната фаза, се користат средни или високи дози на глукокортикоиди.
6. Полимиозитис и дерматомиозитис - глукокортикоиди се лекови по избор. Во акутната фаза, се пропишуваат високи дози на глукокортикоиди.
7. Системска склеродермија - глукокортикоиди се препишуваат во ниски и средни дози со развој на миозитис.
8. Сеуште е болест - во акутна фаза, како и кога во патолошкиот процес се вклучени витални органи и системи (миокардитис, перикардитис, епилепсија) - средни или високи дози на глукокортикоиди.
1.Артеритис на гигантски клетки - во акутна фаза, глукокортикоидите се третман по избор и се препишуваат во високи дози.
2. болест Такајасу - во акутна фаза, се користат средни или високи дози на глукокортикоиди.
3. Нодуларен полиартитис и микроскопски полиангитис - во акутна фаза, се користат високи дози на глукокортикоиди.
4. Вегенерова болест - во акутна фаза - високи дози на глукокортикоиди.
5. Синдром на полнење-Штраус - избор на акутна фаза на терапија - високи дози на глукокортикоиди.
6. Синдром на Бехет - во акутна фаза, се пропишани средни или високи дози на глукокортикоиди.
7. Кожен леукоцитокластичен васкулитис - во тешки случаи, се користат високи дози на глукокортикоиди.
8. Хеморагичен васкулитис (Shenlein-Genoch purpura) - глукокортикоиди се препишуваат во средни или високи дози со развој на гломерулонефритис со нефротски синдром и / или формирање на 50-60% од гломерули и повеќе од половина месечина. Според голем број на ревматолози, просечни дози на глукокортикоиди може да се користат за абдоминален синдром.
1.Гломерулонефритис со минимални промени (идиопатски нефротски синдром) - во почетните фази на болеста или со неговите егзацербации, глукокортикоидите пропишани во средни или високи дози се третман по избор.
2. Фокусно-сегментална гломерулосклероза-хијалиноза - во почетните фази на болеста или со егзацербации, се користат средни или високи дози на глукокортикоиди.
3. Месангиопролиферативен гломерулонефритис користи средни или високи дози на глукокортикоиди со развој на нефротски синдром и / или полумесечина во гломерули од 50-60%.
4. Месангоокапиларен гломерулонефритис - високи дози на глукокортикоиди се користат за развој на нефротски синдром и / или полумесечина во гломерули од 50-60%.
5. Мембранозен гломерулонефритис - во присуство на нефротски синдром, се користат средни или високи дози на глукокортикоиди.
6. Брзо напредувачки гломерулонефритис (субакутен, луннат) - Се користат високи дози на глукокортикоиди.
Секундарниот гломерулонефритис (т.е. гломерулонефритис кој се разви со СЛЕ, ревматоиден артритис, полимиозитис, дерматомиозитис, васкулитис) користат средни или високи дози на глукокортикоиди.
1.Недостаток на ACTH кај разни заболувања на хипофизата - хидрокортизон или алтернативно ниски дози на глукокортикоиди се користи како терапија за замена.
2. Тиротоксикоза предизвикана од амиодарон - се користат високи дози на глукокортикоиди.
3. Инсуфициенција на надбубрежната жлезда - хидрокортизон или алтернативно ниски или средни дози на глукокортикоиди се користат како терапија за замена.
1.Кронова болест - во акутна фаза, се користат високи дози на глукокортикоиди.
2. Неспецифичен улцеративен колитис - во акутна фаза се користат средни или високи дози на глукокортикоиди.
3. Автоимун хепатитис - се користат средни или високи дози на глукокортикоиди.
4. Почетна фаза на цироза - нанесете просечна доза на глукокортикоиди.
5. Тежок алкохолен хепатитис - се користат средни или високи дози на глукокортикоиди.
1.Пропишани се пост-вирусни и неспецифични лимфоцитни миокардитис - средни или високи дози на глукокортикоиди.
2. Акутен не-гноен перикардитис со акумулација на ексудат - се користат средни или високи дози на глукокортикоиди.
1.Бронхијална астма - орални глукокортикоиди (средни или високи дози) се пропишани за акутна тешка астма, сериозни егзацербации на астма, при што вдишените глукокортикоиди и бронходилататори се неефикасни.
2. Криптогени фиброзирачки алвеолитис - се користат високи дози на глукокортикоиди.
3. Омаловажувачки бронхиолитис - се користат високи дози на глукокортикоиди.
4. Саркоидоза на белите дробови - се користат средни или високи дози на глукокортикоиди.
5. Еозинофилна пневмонија - се пропишани средни или високи дози на глукокортикоиди.
1.Се користат хемобластози - високи и многу високи дози на глукокортикоиди.
2. Се користат анемија (хемолитичка, автоимуна, апластична) - се користат средни и високи дози на глукокортикоиди.
3. Тромбоцитопенија - пропишани се средни и високи дози на глукокортикоиди.
1. Шок со различно потекло - користете високи и многу високи дози на глукокортикоиди. Се претпочита пулсна терапија.
2. Алергиски реакции - високи и многу високи дози на глукокортикоиди се пропишани, доколку е потребно, "пулсна терапија".
3. Синдром на акутна респираторна дистрес - се користат многу високи дози на глукокортикоиди.
1.Во зависност од клиничката состојба, се користат глукокортикоиди од ниски до многу високи дози и, доколку е потребно, „пулсна терапија“.
4.Основно нанесакани ефекти на глукокортикоиди
Со кратки курсеви на третман со глукокортикоиди, обично не се појавуваат сериозни несакани ефекти. Некои пациенти пријавуваат зголемување на апетитот, зголемување на телесната тежина, нервозна раздразливост и нарушувања на спиењето.
Со долгорочно администрирање на кортикостероиди, таканаречениот синдром Истенко-Кушинг се развива со тешка дебелина, лице во форма на месечина, прекумерен раст на косата на телото и зголемен крвен притисок. Со намалување на дозата на хормоните, овие феномени се реверзибилни. Најопасниот ефект на глукокортикоиди врз мукозната мембрана на гастроинтестиналниот тракт: тие можат да предизвикаат чирови на дуоденумот и желудникот. Затоа, присуството на пациент со пептичен улкус е една од главните контраиндикации за употреба на кортикоиди. Кога пациентот зема стероидни хормони, ако има поплаки за тежина или болка во горниот дел на стомакот, металоиди, потребно е да се препишат лекови кои ја намалуваат киселоста на желудечниот сок. Третманот со какви било глукокортикоиди е придружена со губење на калиум, така што земањето преднизон мора да се комбинира со земање препарати од калиум (паангин, аспаркум). Кортикостероидите предизвикуваат задржување на натриум и течности во организмот, така што кога се појавува едемот, може да се користат само диуретици кои штедат калиум (на пример, триапур, триаголник К). Со продолжено администрирање на кортикостероиди кај деца, можно е нарушување на растот и одложен пубертет.
Сите глукокортикоиди имаат слични несакани ефекти, кои зависат од дозата и времетраењето на третманот.
1. Задушување на функцијата на надбубрежниот кортекс. Глукокортикоидите ја потиснуваат функцијата на системот на хипоталамус-хипофиза-надбубрежниот кортекс. Овој ефект може да трае со месеци по прекинот на третманот и зависи од употребената доза, фреквенцијата на администрација и времетраењето на терапијата. Ефектот врз кората на надбубрежната жлезда може да се ослабне ако наместо лекови со долго дејство (дек-метазон), се користат лекови со кратко дејство, како што се преднизон или метилпреднизолон во мали дози. Препорачливо е да се земе целата дневна доза во раните утрински часови, што е најсоодветно со физиолошкиот ритам на секреција на ендоген кортизол. Кога се зема секој втор ден, се користат глукокортикоиди со кратко дејство и се пропишува и единечна доза во раните утрински часови. Под влијание на стресови (операции на стомакот, сериозни акутни истовремени заболувања, итн.), Хипофункцијата на надбубрежниот кортекс често се манифестира, манифестирана со недостаток на апетит, губење на тежината, поспаност, треска и ортостатска хипотензија. Зачувана е минералокортикоидна функција на надбубрежниот кортекс, затоа, хиперкалемија и хипонатремија, карактеристични за примарна надбубрежна кортикална инсуфициенција, обично се отсутни. Пациентите треба да носат специјална нараквица или да имаат лекарска картичка со нив, така што во итен случај, лекарот знае за потребата од итно администрирање на глукокортикоиди. Кај пациенти кои земаат неколку недели повеќе од 10 мг преднизон на ден (или еквивалентна доза на друг лек), еден или друг степен на сузбивање на надбубрежниот кортекс може да трае и до 1 година по прекинување на третманот.
2. Задушување на имунитетот.Глукокортикоидите ја намалуваат отпорноста на инфекции, особено бактериските, ризикот од инфекција директно зависи од дозата на глукокортикоиди и останува главна причина за компликации и смрт на пациенти со СЛЕ. Како резултат на третман на стероид, локална инфекција може да стане системска, латентна инфекција може да стане активна, а непатогените микроорганизми исто така можат да го предизвикаат. Наспроти позадината на терапијата со глукокортикоидна инфекција може да се појави тајно, но телесната температура обично се зголемува. Како превентивна мерка се препорачува имунизација со вакцини против грип и пневмококни, кои не предизвикуваат егзацербација на СЛЕ. Пред да започнете со третман со глукокортикоиди, препорачливо е да се спроведе тест за туберкулин на кожата.
3. Промените во изгледот вклучуваат: заокружување на лицето, зголемување на телесната тежина, прераспределување на телесните масти, хирзутизам, акни, виолетови стрии, модринки со минимални повреди. Овие промени се намалуваат или исчезнуваат по намалувањето на дозата.
4. Менталните нарушувања се движат од блага раздразливост, еуфорија и нарушувања на спиењето до тешка депресија или психоза (последното може погрешно да се смета како лепус лезија на централниот нервен систем).
5. Хипергликемија може да се појави или да се зголеми за време на третманот со глукокортикоиди, но, како по правило, не служи како контраиндикација за нивно назначување. Може да биде потребна употреба на инсулин, ретко се развива кетоацидоза.
6. Прекршувања на билансот на вода-електролит вклучуваат задржување на натриум и хипокалемија. Посебни тешкотии во третманот се појавуваат со конгестивна срцева слабост и едем.
7. Глукокортикоидите можат да предизвикаат или зголемат артериска хипертензија. I / O пулсна терапија со стероиди често ја влошува постојната артериска хипертензија ако е тешко да се лекува.
8. Остеопенија со фрактури на компресија на вертебралните тела често се развива со продолжена терапија со глукокортикоид. Затоа, пациентите треба да примаат калциумови јони (1-1,5 g / ден по уста). Диуретиците со витамин Д и тиазид може да бидат корисни. Кај жени во постменопауза, со зголемен ризик од остеопенија, обично се прикажани естрогени, но резултатите од нивната употреба во СЛЕ се контрадикторни. Може да се користат и калцитонити и дифосфонати. Се препорачува вежби за стимулирање на остеогенезата.
9. Стероидна миопатија се карактеризира со оштетување на мускулите главно на рамото и карличната појас. Забележана е мускулна слабост, но нема болка, активноста на крвните ензими од мускулно потекло и електромиографските параметри, за разлика од воспалителното оштетување на мускулите, не се менува. Биопсија на мускулите се спроведува само во ретки случаи кога е неопходно да се исклучи нивното воспаление. Можноста за стероидна миопатија се намалува бидејќи дозата на глукокортикоиди се намалува и се изведува комплекс на интензивни физички вежби, сепак, целосното закрепнување може да трае неколку месеци.
10. Офталмолошките нарушувања вклучуваат зголемен интраокуларен притисок (што понекогаш се должи на прогресија на глауком) и задниот субкапсуларен катаракта.
11. Исхемична некроза на коските (асептична, аваскуларна некроза, остеонекроза) може да се појави и за време на терапија со стероиди. Овие компликации се честопати повеќекратни, со оштетување на бедрената глава и хумерус, како и на платото на тибија. Раните абнормалности се откриени со изотопична сцинтиграфија и МНР. Појавата на карактеристични радиолошки промени укажува на далекусежен процес. Хируршката декомпресија на коските може да биде ефективна во раните фази на исхемична некроза, но проценките на овој метод на лекување се контроверзни.
12. Другите несакани ефекти на глукокортикоиди вклучуваат хиперлипидемија, менструални неправилности, зголемено потење, особено во текот на ноќта и бенигна интракранијална хипертензија (pseudotumor cerebri). Дејството на глукокортикоиди понекогаш е поврзано со појава на тромбофлебитис, некротизирачки артеритис, панкреатитис и чир на пептик, но доказите за оваа врска се недоволни.
5.Предупредување за чукањеглукокортикоиди
1. Јасна причина за употреба на глукокортикоиди.
2. Образложениот избор на глукокортикоиден лек, кој се карактеризира со висока ефикасност и релативно низок спектар на несакани ефекти. Метилпреднизолон (Медрол, Солу-медрол и Депо-медрол) ги исполнува овие барања, аргументите за кои се дадени погоре.
3. Изборот на почетната доза на глукокортикоиден лек кој го обезбедува потребниот клинички ефект при неговите минимални дози треба да се заснова на детална проценка на пациентот, вклучително и нозологијата на болеста, нејзината активност, присуство на оштетување на виталните органи и системи, како и општо прифатените препораки во тактиката на глукокортикоидна терапија за разни клинички ситуации. Денес, глукокортикоидната терапија е недвосмислено препознаена како третман на избор за многу ревматски заболувања, вклучително и СЛЕ, дерматомиозитис и полимиозитис, васкулитис, гломерулонефритис и многу повеќе. Во исто време, почетните дози значително се разликуваат во зависност од карактеристиките на клиничката слика и лабораториските параметри. Така, на пример, со висока активност на СЛЕ, дерматомиозитис, полимиозитис, системски васкулитис и / или вклучување на витални органи и системи во овие болести, индицирана е употреба на високи или многу високи дози на глукокортикоиди. Во исто време, со мала активност на СЛЕ, васкулитис, добар клинички ефект може да се постигне со ниски дози на глукокортикоиди, а во отсуство на оштетување на внатрешните органи и централниот нервен систем, не е неопходно да се препише глукокортикоидна терапија за да се постигне клиничка ремисија, бидејќи може да се постигне доволен клинички ефект со користење на НСАИЛ , обично во комбинација со препарати со аминокинолин. Во исто време, голем број на пациенти имаат потреба од дополнителна употреба на ниски дози на глукокортикоиди (Медрол 4-6 мг на ден или преднизолон 5-7,5 мг на ден).
Распространетата употреба на лекови за менување на болести веќе во раните фази на ревматоиден артритис, недостаток на податоци за позитивните ефекти на средни и високи дози на глукококортикоиди врз долгорочната прогноза кај пациенти со ревматоиден артритис, како и високиот ризик од сериозни несакани ефекти при нивно користење, значително ги променија приодите кон употреба на глукокортикоиди. Денес во отсуство
Сериозни вон-артикуларни манифестации на ревматоиден артритис (на пример, васкулитис, пневмонитис) не се препорачуваат за употреба на глукокортикоиди во дози кои надминуваат 7,5 мг на ден на преднизон или 6 мг метилпреднизолон. Покрај тоа, кај многу пациенти со ревматоиден артритис, додавањето на 2-4 mg на ден на Medrol на терапијата за менување на болеста се карактеризира со добар клинички ефект.
1. Воспоставете техника за земање глукокортикоиди: континуирани (дневни) или наизменични (алтернативни и наизменични) опции.
2. Кај повеќето ревматски заболувања, васкулитис, гломерулонефритис, глукокортикоиди обично не се доволни за да се постигне целосна или делумна клиничка и лабораториска ремисија, за што е потребна нивна комбинација со разни цитотоксични лекови (азатиоприн, циклофосфамид, метотрексат и други). Покрај тоа, употребата на цитостатици може значително да ја намали дозата на глукокортикоиди (па дури и да ги откаже), додека да го задржи добиениот клинички ефект, со што значително се намалува фреквенцијата и сериозноста на несаканите ефекти на терапијата со глукокортикоиди.
3. Многу клиничари препорачуваат да се продолжи со долготрајни многу ниски дози на глукокортикоиди (2-4 mg / ден на Medrol® или 2,5-5,0 mg / ден на преднизолон) кај многу пациенти со ревматски заболувања по постигнување клиничка и лабораториска ремисија.
Сосписок на користена литература
1 предавање Д-р, проф. Д-р Лобанова Е.Г. Чекалина Н.Д.